Osteoporose ist ein Thema, das alle betrifft – als ÄrztInnen und PatientInnen. Jede dritte Frau wird im Laufe ihres Lebens eine Fragilitätsfraktur erleiden. Auch Männer sind betroffen. Deshalb wäre es einerseits notwendig, Betroffene mit schon bestehender Fragilitätsfraktur zu therapieren, aber andererseits sinnvoll, jene frühzeitig zu diagnostizieren und zu therapieren, die an Osteoporose leiden, aber sich noch nichts gebrochen haben, damit sie sich Fragilitätsfrakturen in weiterer Folge ersparen. Aktuelle Daten weisen darauf hin, dass derzeit viel zu wenig therapiert wird – es gibt diesbezüglich eine große Behandlungslücke. Eine Studie in acht Ländern in Europa ergab, dass etwa 75% der älteren Frauen, bei denen ein hohes Risiko für Fragilitätsfrakturen bestand, keine geeignete Therapie erhielten 1. Die fehlende Diagnose scheint dabei ein wichtiger Faktor zu sein, denn von den Personen, die ein erhöhtes Risiko einer Fragilitätsfraktur hatten und keine Therapie erhielten, hatten 94% auch keine Diagnose. In Österreich liegt die Behandlungslücke sogar bei 80%, denn nur 20% der PatientInnen werden gemäß der ICUROS Studie nach Fraktur im Krankenhaus antherapiert 2. Auch im niedergelassenen Bereich werden diese PatientInnen in der Regel nicht aufgefangen, denn in der Nachbeobachtungsphase der ICUROS Studie waren nach 18 Monaten nur 10% der Männer und 15% der Frauen auf eine entsprechende Osteoporosetherapie eingestellt. Auch werden die 20% PatientInnen, die im Spital antherapiert wurden, in der Folge oft nicht weiter behandelt, obwohl die Osteoporose eine chronische Erkrankung ist. Nur 56% der Männer und 60% der Frauen, die mit einer Osteoporosetherapie das Spital verlassen hatten, waren nach 18 Monaten noch in Behandlung. Die Diagnose einer Osteoporose wird daher insgesamt zu selten gestellt und wenn sie gestellt ist, dann werden die PatientInnen nur in einem geringen Ausmaß behandelt.
Die Knochendichtemessung als Beurteilungsmethode für die Diagnose und Therapie der Osteoporose ist allein nicht ausreichend. Ein durch die DEXA Messung kalkulierter T-Score < -2,5 reicht nicht aus, um eine Osteoporose zu definieren. Dies entspricht nicht immer dem Grenzwert, ab dem in der klinischen Realität eine Osteoporosetherapie eingeleitet werden sollte 3, dafür sollte eine Mikrostrukturveränderung im Knochen vorliegen. Knochendichte-Ergebnisse müssen daher differenziert beurteilt werden.
So zeigte z.B. eine Studie, dass bei 28% der postmenopausalen Frauen im Röntgen Wirbelkörperfrakturen festgestellt wurden, die sich bis zum Zeitpunkt der Studie quasi als gesund betrachtet hatten. Die daraufhin durchgeführte Knochendichtemessung (DEXA) wies jedoch keine Korrelation zwischen kalkulierten T-Score Werten in der Lendenwirbelsäule und Häufigkeit der Wirbelkörperfrakturen auf 4. Die Prävalenz der Lendenwirbelfrakturen hing lediglich mit dem Alter und der Knochendichte in der Hüfte zusammen.
Osteoporose ist definiert als eine Verringerung der Knochenmasse und der Knochenstruktur. (5). Die Knochenqualität hängt von vielen Faktoren ab, nicht nur von der Knochenmineralisation (gemessen durch die DEXA). Weitere Faktoren umfassen höheres Alter, weibliches Geschlecht, Knochenumbau, Medikamenteneinfluss, toxische Einflüsse wie Rauchen und Alkohol, Aromatasehemmer, und vieles mehr. Der wesentliche Behandlungsansatz sollte daher sein, die Knochenqualität zu verbessern, nicht die Knochendichte, um die Knochenfestigkeit zu verbessern.
Eine generelle Indikation für eine Osteoporosetherapie ist gemäß der DVO Leitlinie aus 2017 5 gegeben bei einer Fragilitätsfraktur des Wirbelkörpers, des Schenkelhalses oder generell bei langfristiger Glukokortikoid-Therapie (abhängig von der Dosis). Ist keine dieser drei generellen Indikationen erfüllt, ist es sinnvoll, das Frakturrisiko mittels Frakturrisiko-Kalkulatoren zu ermitteln, um Risikopersonen frühzeitig zu identifizieren. Somit kann bereits im Vorfeld eine spezifische Therapie eingeleitet werden, um Frakturen in der Zukunft zu verhindern.
Das Ziel bei Osteoporose ist die Prävention von Sekundärfolgen, also in diesem Falle einer Fragilitätsfraktur. Denn eine Fragilitätsfraktur ist nicht harmlos! Innerhalb eines Jahres nach einer Schenkelhalsfraktur versterben 20% der Patientinnen und 33% der PatientInnen an den Folgen 6. Auch können mit der Verhinderung von Fragilitätsfrakturen wesentliche Folgekosten eingespart werden. Man weiß, dass in Österreich besonders die Zahl der Hüftfrakturen hoch ist – höher als in anderen Ländern, auch höher als in Deutschland. Österreich führt in Bezug auf Fragilitätsfrakturen zusammen mit Schweden und Dänemark die Statistik an.7
Bei klassischen osteoporotischen Frakturen, z.B. niedrigtraumatischen Wirbel- oder Schenkelhalsfrakturen, empfiehlt die DVO Leitlinie 5, rasch eine Therapie einzuleiten. Schenkelhalsfrakturen sind klinisch einfacher zu diagnostizieren, osteoporotische Wirbelkörperfrakturen verursachen oft lediglich unspezifische Rückenschmerzen und werden, wenn eine Bildgebung veranlasst wird, oft im radiologischen Befund nicht erwähnt 8. Deshalb ist es ratsam, bei älteren PatientInnen auf die indirekten Zeichen einer Wirbelfraktur zu achten, nämlich neue oder vorübergehende Rückenschmerzen, Verlust an Körpergröße, erhöhter Hinterkopf-Wand-Abstand und verringerter Abstand zwischen Rippen und Becken 9-11.
In Bezug auf die Glukokortikoidtherapie stellt gemäß DVO Leitlinie 5 bereits eine orale Gabe von ≥7,5 mg täglich über drei Monate eine Indikation für eine Osteoporosetherapie dar, wenn der T-Score im osteopenischen Bereich liegt oder wenn schon eine Fragilitätsfraktur vorliegt.
Bei niedrigeren Glukokortikoiddosen, sollte das Frakturrisiko mit dem FRAX Tool (Risikorechner) oder gemäß DVO Risikokategorisierung bestimmt werden 12. In Österreich bleibt es der behandelnden Ärztin/dem behandelnden Arzt überlassen, welches Instrument zur Risikoabschätzung zum Einsatz kommt. Gemäß FRAX kann schon ein T-Score, der im Bereich der Osteopenie liegt, bei Frauen mit positiver Familienanamnese ein stark erhöhtes Frakturrisiko bedeuten. Es wird diskutiert, dass bereits ab einem Risiko für eine „major osteoporotic fracture“ von 20% und einem Hüftfrakturrisiko von 5% eine Osteoporosetherapie eingeführt werden soll. Auch die DVO Leitlinie berücksichtigt bei der Risikoabschätzung ein ganzes Konvolut an Risikofaktoren.
Für den Nutzen einer Anti-Osteoporose-Medikation ist der Zeitpunkt der Initiierung von entscheidender Bedeutung. Bei einer Behandlungsinitiierung rasch nach einer Hüftfraktur kann das Risiko, erneut mit einer Fraktur hospitalisiert zu werden, signifikant gesenkt werden 13. Das Risiko einer Folgefraktur ist innerhalb der ersten Jahre nach einer klinischen Fraktur bis zu fünffach erhöht, aber selbst nach 15 Jahren ist das Risiko einer Folgefraktur noch doppelt so hoch, wenn man nichts dagegen tut 14.
Grundsätzlich entscheidet sich die Wahl des geeigneten Therapeutikums nach dem Frakturrisiko 15.
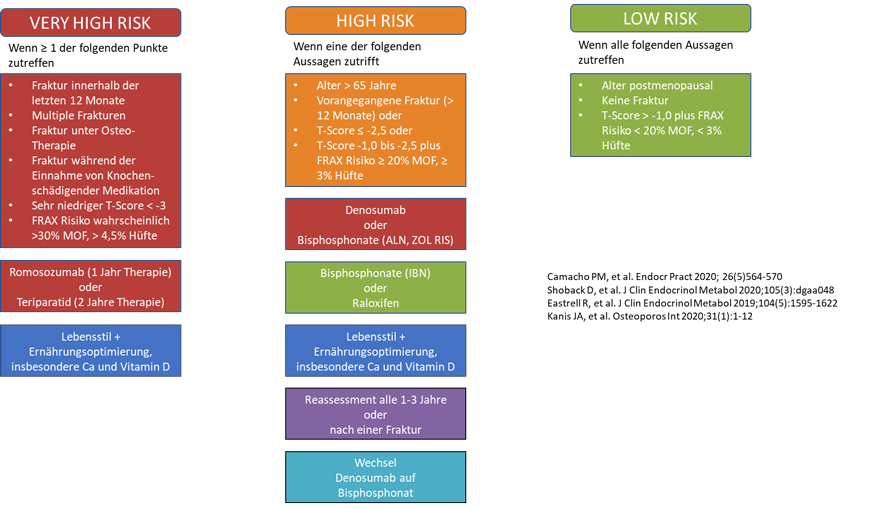
PatientInnen mit sehr hohem Knochenbruch-Risiko sollten hinsichtlich des Lebensstils und einer etwaigen Ernährungsoptimierung, insbesondere Kalzium und Vitamin D, beraten werden und eine knochenanabole (=Knochenaufbau/Osteoblasten-stimulierende) Therapie erhalten. Wo verfügbar und indiziert sollte Romosozumab gegeben werden, ansonsten Teriparatid. Es hat sich gezeigt, dass eine knochenanabole Therapie firstline effektiver ist als nach einer antiresorptiven (= Knochenabbau/Osteoklasten-hemmende) Therapie. Denosumab oder Bisphosphonate, als antiresorptive Medikation, können firstline gegeben werden, wenn Romosozumab und Teriparatid kontraindiziert sind oder nicht selbst verabreicht werden können. Wichtig zu wissen ist, dass Teriparatid nur etwa zwei Jahre lang wirkt. Danach muss eine antiresorptive Therapie angeschlossen werden, um die aufgebaute Knochenmasse zu erhalten.
Bei PatientInnen mit hohem Risiko wird leitlinienkonform ebenfalls eine Lebensstiländerung empfohlen und eine Gabe von Denosumab oder alternativ parenteralen Bisphosphonaten eingeleitet. Orale Bisphosphonate haben eine schlechtere Bioverfügbarkeit und rufen gastrointestinale Nebenwirkungen hervor. Parenterale Bisphosphonate zeigen bei Langzeitgabe einen fehlenden weiteren Knochendichte-Anstieg. Wichtig ist, die Osteoporosetherapie nicht abzubrechen, wenn das Frakturrisiko weiterhin erhöht ist. Es zahlt sich hingegen aus, Medikamente bei Unverträglichkeit oder fehlender Effektivität zu wechseln, denn das Frakturrisiko gehört weiterhin langfristig gesenkt. Auf Basis von unabhängigen Studien 16,17 sollte Denosumab diesbezüglich der Vorzug gegeben werden. Die Knochenhistologie verändert sich nach Langzeitgabe von Denosumab nicht 18. Wenn man Denosumab absetzt, geht die Wirksamkeit allerdings relativ rasch, bereits nach 6 Monaten, verloren 19. Der Grund ist, dass Osteoklasten nach Aufhebung der Hemmung eine erhöhte Aktivität zeigen. Dieser sogenannte Rebound kann bis zu einem Jahr anhalten und führt wieder zum Knochenabbau.
In der Osteoporosetherapie mit Denosumab gilt:
Nach längerer Behandlungsdauer und bei hohem Frakturrisiko sollte man Denosumab nach Möglichkeit weiterführen. Wird Denosumab dennoch abgesetzt, gelten folgende Regeln 20: Wenn Denosumab bei PatientInnen mit geringem Frakturrisiko nach kurzer Dauer, z.B. 2,5 Jahren, abgesetzt wird, kann man zur Erhaltung der Wirkung über 1-2 Jahre orale Bisphosphonate oder Zoledronsäure verabreichen. Wenn Denosumab bei PatientInnen nach längerer Dauer gestoppt wird, sollte man nach 6 Monaten eine Injektion von Zoledronsäure verabreichen.
Als Grund für ein Absetzen von Denosumab wird oft die Sorge vor einer Kieferosteonekrose (ONJ) im Zug einer Zahnbehandlung genannt. Hier kann man beruhigen. Das Risiko von ONJ ist bei PatientInnen mit Osteoporose, die eine antiresorptive Therapie erhalten, mit 0,001% - 0,01% annähernd gleich hoch wie in der Allgemeinbevölkerung 21. ONJ tritt in der Allgemeinbevölkerung auch ohne antiresorptive Therapie auf und heilt normalerweise innerhalb von 12 Wochen ab.
Es besteht auf Basis von Langzeiterfahrungen kein Grund, dass in dieser Situation eine Therapieunterbrechung angezeigt wäre. Die folgenden Risikofaktoren sollten bei der Einschätzung des Risikos des Patienten/der Patientin für die Entwicklung von ONJ berücksichtigt werden:
- Krebs, Begleiterkrankungen (z. B. Anämie, Koagulopathien, Infektionen), Rauchen.
- Begleittherapien: Kortikosteroide, Chemotherapie, Angiogeneseinhibitoren, Radiotherapie im Kopf-Hals-Bereich.
- Schlechte Mundhygiene, Erkrankungen des Zahnfleisches, schlecht sitzende Zahnprothesen, vorbestehende Zahnerkrankungen, invasive Zahnbehandlungen (z. B. Zahnextraktionen). Alle PatientInnen sollten dazu angehalten werden, eine gute Mundhygiene einzuhalten.
Österreich ist Spitzenreiter bei Fragilitätsfrakturen der Hüfte. Die Gründe sind multifaktoriell aber im Detail nicht verstanden. Ein wesentlicher Faktor ist sicher die große Behandlungslücke hierzulande. Wichtig ist daher, die Diagnose einer Osteoporose zu stellen und adäquat zu therapieren. Nicht nur die Knochendichte ist für die Diagnose relevant, sondern eine Vielzahl an Faktoren, allen voran das Alter und das Geschlecht. Osteoporose ist kein Schicksal, sondern eine behandelbare Erkrankung. Die Therapie sollte individuell, nach Risiko und vor allem rasch erfolgen, um eine hohe Effektivität zu erreichen.
